 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)


在标准压力100kPa和373K时,把1molH2O(g)可逆压缩为液体,计算该过程的W,Q,△U,△H。已知该条件下水的蒸发热为22
在标准压力100kPa和373K时,把1molH2O(g)可逆压缩为液体,计算该过程的W,Q,△U,△H。已知该条件下水的蒸发热为2258kJ·kg-1,已知M(H2O)=18.0g·mol-1,水蒸气可视为理想气体。

 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)


在标准压力100kPa和373K时,把1molH2O(g)可逆压缩为液体,计算该过程的W,Q,△U,△H。已知该条件下水的蒸发热为2258kJ·kg-1,已知M(H2O)=18.0g·mol-1,水蒸气可视为理想气体。

 更多“在标准压力100kPa和373K时,把1molH…”相关的问题
更多“在标准压力100kPa和373K时,把1molH…”相关的问题
在373K、压力为100kPa时,1.0g H2O(l)经下列不同的过程变为373K、100kPa的H2O(g),请分别求出各个过程的△U、△H、W和Q。
(1)在373K、100kPa压力下H2O(l)变成同温、同压的汽;
(2)先在373K、外压为50kPa下变为汽,然后可逆加压成373K、100kPa的汽;
(3)把H2O(l)突然放进恒温373K的真空箱中,控制容积使终态为100kPa的汽。已知水的汽化热为2259kJ·kg-1。
已知在373K和100kPa压力时,1kgH2O(l)的体积为1.043dm3,1kg H2O(g)的体积为1677dm3,H2O(l)的摩尔汽化热△vapHm=40.69kJ·mol-1。当1mol H2O(l)在373K和外压100kPa时完全蒸发成H2O(g)。(1)试求蒸发过程中系统对环境所做的功;(2)假定液态水的体积可忽略不计,试求蒸发过程中系统对环境所做的功,并计算所得结果的相对误差;(3)假定把蒸汽看做理想气体,且略去液态水的体积,求系统所做的功;(4)求(1)中变化的△vapUm和△vapHm;(5)解释何故蒸发的焓变大于系统所做的功。
在298.15K及100kPa压力时,设环丙烷、石墨及氢的燃烧焓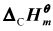 (298.15K)分别为-2092kJ·mol-1、-393.8kJ·mol-1及-285.84kJ·mol-1。若已知丙烯C3H6(g)的标准摩尔生成焓
(298.15K)分别为-2092kJ·mol-1、-393.8kJ·mol-1及-285.84kJ·mol-1。若已知丙烯C3H6(g)的标准摩尔生成焓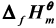 =20.50kJ·mol-1,试求:(1)环丙烷的标准摩尔生成焓
=20.50kJ·mol-1,试求:(1)环丙烷的标准摩尔生成焓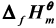 (298.15K);(2)环丙烷异构化为丙烯的摩尔反应焓变值
(298.15K);(2)环丙烷异构化为丙烯的摩尔反应焓变值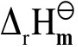 (298.15K)。
(298.15K)。
 Cp,m(H2,g)=29.07J·mol-1·K-1+(8.36×10-4J·mol-1·K-2)T
Cp,m(H2,g)=29.07J·mol-1·K-1+(8.36×10-4J·mol-1·K-2)T
Cp,m(O2,g)=36.16J·mol-1·K-1+(8.45×10-4J·mol-1·K-2)T
Cp,m(H2O,g)=30.00J·mol-1·K-1+(10.7×10-3J·mol-1·K-2)T
Cp,m(H2O,l)=75.26J·mol-1·K-1
在标准压力100kPa下,乙醇(A)和乙酸乙酯(B)二元液相系统的组成与温度的关系如下表所示:
T/K | 351.5 | 349.6 | 346.0 | 344.8 | 345.0 | 348.2 | 350.3 |
xB | 0 | 0.058 | 0.290 | 0.538 | 0.640 | 0.900 | 1.000 |
yB | 0 | 0.120 | 0.400 | 0.538 | 0.602 | 0.836 | 1.000 |
乙醇和乙酸乙酯的二元液相系统有一个最低恒沸点。请根据表中数据:
(1)画出乙醇和乙酸乙酯的二元液相系统的T-x-y图;
(2)将纯的乙醇和纯的乙酸乙酯混合后加到精馏塔中,经过足够多的塔板,在精馏塔的顶部和底部分别得到什么产品?
光气分解反应COCl2(g)====CO(g)+Cl2(g)在373K时,K=8.80×10-9求在373K平衡后总压力P总=202.6KPA光气的解离度?
在600K、100kPa压力下,生石膏的脱水反应为
CaSO4·2H2O(s)===CaSO4(s)+2H2O(g)
试计算该反应进度为1mol时的Q、W、△Um、△Hm、△Sm、△Am及△Gm。已知各物质在298K、100kPa的热力学数据如下表所示:
物质 | frac{Delta_{f}H_{m}^{Theta }}{kJcdot mol^{-1}} | frac{S_{m}^{Theta }}{Jcdot mol^{-1}cdot K^{-1}} | frac{C_{p,m}}{Jcdot mol^{-1}cdot K^{-1}} |
CaSO4·2H2O(s) | -2021.12 | 193.97 | 186.20 |
CaSO4(s) | -1432.68 | 106.70 | 99.60 |
H2O(g) | -241.82 | 188.83 | 33.58 |