 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)


某固体混合物X可能含有Fe、Fe2O3、CuO、MnO2、NaCl和K2CO3中的几种,进行了以下实验:①X溶于足量水中,得到固体Y和弱碱性溶液Z。②取固体Y,加足量浓盐酸,加热,产生无色气体,析出红色固体,得溶液W。下列结论正确的是()。
A、X中一定不存在Fe2O3、MnO2
B、X中一定含有Fe、CuO和K2CO3
C、往溶液Z中加入AgNO3溶液,若产生白色沉淀,则Z中含NaCl
D、取溶液W,加少盐NaOH溶液,肯定产生沉淀

 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)


A、X中一定不存在Fe2O3、MnO2
B、X中一定含有Fe、CuO和K2CO3
C、往溶液Z中加入AgNO3溶液,若产生白色沉淀,则Z中含NaCl
D、取溶液W,加少盐NaOH溶液,肯定产生沉淀

 更多“某固体混合物X可能含有Fe、Fe2O3、CuO、…”相关的问题
更多“某固体混合物X可能含有Fe、Fe2O3、CuO、…”相关的问题
A、2.8g
B、5.6g
C、11.2g
D、无法计算
A、滤液有两种可能的组成
B、滤液中滴加稀盐酸,有白色沉淀产生
C、滤渣中至少有两种物质
D、滤渣中滴加稀盐酸,一定有气泡产生
A、Cu(NO3)2
B、Fe(NO3)3
C、Fe(NO3)2
D、Fe(NO3)2和Cu(NO3)2
A、滤渣中一定不含单质铁
B、滤液中一定含有 Cu2+
C、滤渣中一定含有银和铜
D、滤液的质量一定大于原溶液的质量
A、原溶液中一定存在的离子:Na+,SO42-,OH
B、原溶液中一定不存在的离子只有Cu2+
C、原溶液中可能存在的离子:SO42-,NO3-
D、红褐色沉淀的化学式为Fe(OH)2
从含镍废催化剂中可回收镍,其流程如下: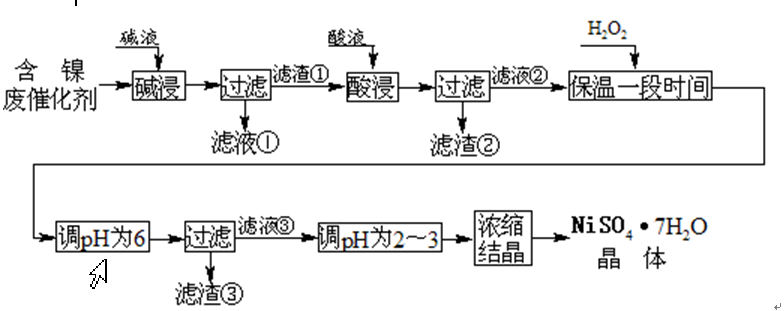 某油脂化工厂的含镍催化剂主要含有Ni,还含有Al(31%)、Fe(1.3%)的单质及氧化物,其他不溶杂质(3.3%)。部分阳离子以氢氧化物形式完全沉淀时的pH如下
某油脂化工厂的含镍催化剂主要含有Ni,还含有Al(31%)、Fe(1.3%)的单质及氧化物,其他不溶杂质(3.3%)。部分阳离子以氢氧化物形式完全沉淀时的pH如下
问题一、碱浸“的目的是除去()。
问题二、“酸浸”时所加入的酸是()(填化学式)。酸浸后,滤液②中可能含有的金属离子是()。
问题三、“调pH为2~3”的目的是()。
问题四、产品晶体中有时会混有少量绿矾(FeSO4•7H2O),可能是由于生产过程中()导致Fe2+未被完全氧化造成的。
问题五、NiSO4在强碱溶液中用NaClO氧化,可制得碱性镍镉电池电极材料——NiOOH。该反应的离子方程式是()