 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)

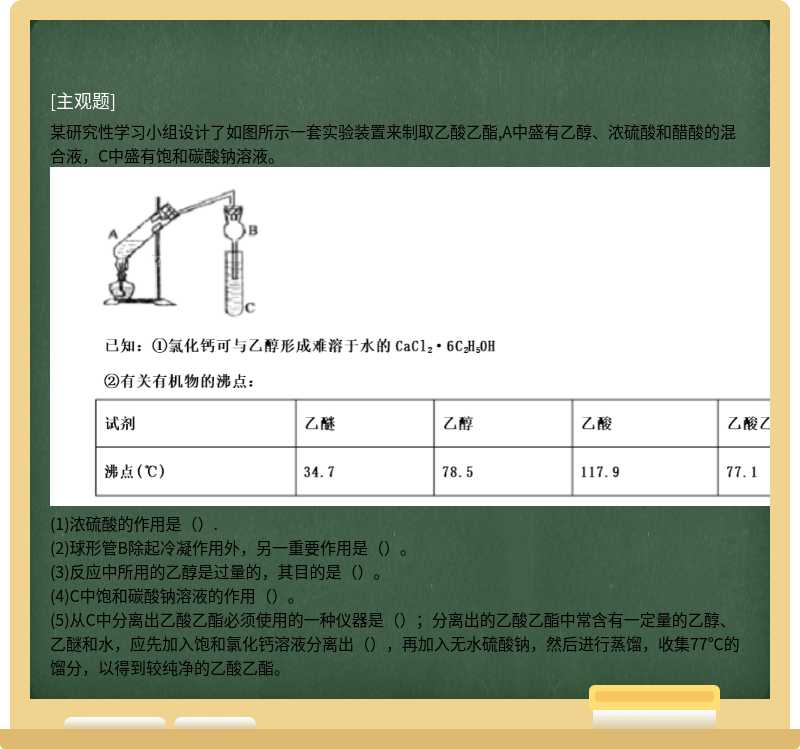
某研究性学习小组设计了如图所示一套实验装置来制取乙酸乙酯,A中盛有乙醇、浓硫酸和醋酸的混合液,C中盛有饱和碳酸钠溶液。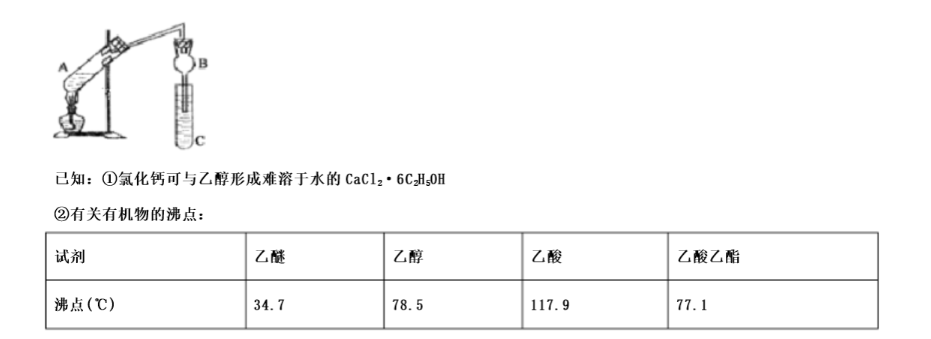 (1)浓硫酸的作用是().
(1)浓硫酸的作用是().
(2)球形管B除起冷凝作用外,另一重要作用是()。
(3)反应中所用的乙醇是过量的,其目的是()。
(4)C中饱和碳酸钠溶液的作用()。
(5)从C中分离出乙酸乙酯必须使用的一种仪器是();分离出的乙酸乙酯中常含有一定量的乙醇、乙醚和水,应先加入饱和氯化钙溶液分离出(),再加入无水硫酸钠,然后进行蒸馏,收集77℃的馏分,以得到较纯净的乙酸乙酯。

 更多“某研究性学习小组设计了如图所示一套实验装置来制取…”相关的问题
更多“某研究性学习小组设计了如图所示一套实验装置来制取…”相关的问题
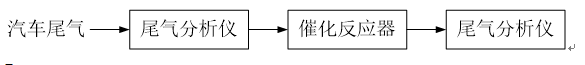
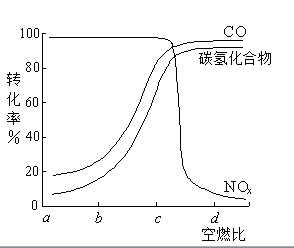
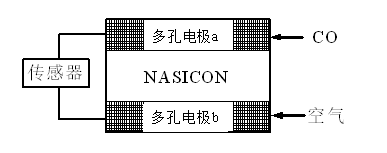
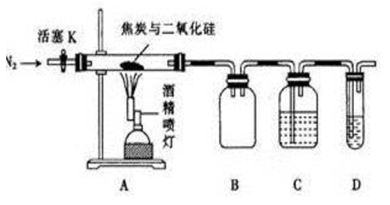 (1)实验时要先通入足够长时间的N2,其原因是()。
(1)实验时要先通入足够长时间的N2,其原因是()。










 如果结果不匹配,请
如果结果不匹配,请 