 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)


从化合价升降的角度判断下列反应()属于氧化还原反应。
A、NaOH+HCl=NaCl+H2O
B、CaCl2+Na2CO3=CaCO3↓+2NaCl
C、2Na+2H2O=2NaOH+H2↑
D、CaO+H2O==Ca(OH)2

 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)


A、NaOH+HCl=NaCl+H2O
B、CaCl2+Na2CO3=CaCO3↓+2NaCl
C、2Na+2H2O=2NaOH+H2↑
D、CaO+H2O==Ca(OH)2

 更多“从化合价升降的角度判断下列反应()属于氧化还原反…”相关的问题
更多“从化合价升降的角度判断下列反应()属于氧化还原反…”相关的问题
A、氧气由氧原子构成
B、反应中氢原子和氧原子都发生了变化
C、反应前后元素的化合价发生了变化
D、水是由氢元素和氧元素组成的化合物
A、次氯酸钠属于氧化物
B、次氯酸钠中钠、氯、氧元素质量比为1:1:1
C、次氯酸钠中氯元素化合价为+1价
D、次氯酸钠是由1个钠原子、1个氯原子和1个氧原子构成
A、金属钠与氯气反应生成氯化钠后,其结构的稳定性增强,体系的能量降低
B、物质燃烧可看作是储存在物质内部的能量(化学能)转化为热能释放出来
C、氮气分子内部存在着很强的化学键,故通常情况下氮气的化学性质很活泼
D、需要加热才能发生的反应不一定是吸收能量的反应
A、不同环境下对重要性的判断可能是不同的
B、重要性概念从会计报表使用者的角度来考虑
C、重要性是注册会计师运用主业判断得来的
D、重要性概念从注册会计师的角度来考虑
从铝+矿(主要成分是Al2O3,含RO2、Fe2O3等杂质)中提取Al2O3的一种工艺流程如图13所示: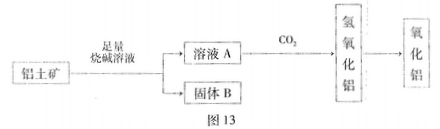
问题一、元素R位于周期表中的第三周期,其最高正化合价和负化合价的绝对值相等。RO2的用途有(写出1条即可)()。
问题二、铝土矿加入足量烧碱溶液后主要反应的离子方程式为
①()。
②()。
问题三、工业上通过电解氧化铝和冰晶石的熔融液来冶炼金属铝。已知电极材料为惰性材料,阳极反应式为()。
问题四、氧化铝与焦炭的混合物在氮气中高温加热反应,制得新型非金属材料AIN与一种中学常见气体X。已知每转移3mole-,有1.5mol化合物X生成,此反应的化学方程式()。
A、原子序数:X>Y>Z
B、非金属性:X>Y>Z
C、原子半径:X>Y>Z
D、最高化合价:X>Y>Z
A、上述反应中,N2是还原剂Al2O3是氧化剂
B、AlN中氮元素的化合价为+3
C、上述反应中,每生成1molAlN需转移3mol电子
D、AlN的摩尔质量为41g