 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)


[判断]
5LNa2SO4溶液中含有2molNa+离子,则溶液中Na+的物质的量的浓度为0.4mol/L()
是
否
查看答案

 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)


是
否

 更多“5LNa2SO4溶液中含有2molNa+离子,则…”相关的问题
更多“5LNa2SO4溶液中含有2molNa+离子,则…”相关的问题
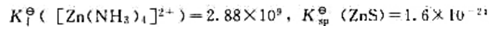
A、溶液甲是由两种物质组成的混合物
B、向溶液甲中滴加氯化钡溶液,一定有白色沉淀产生
C、若操作Ⅱ是滴加适量氢氧化钠溶液、过滤、蒸发结晶,则固体乙是氯化钠晶体
D、若操作Ⅱ是降温结晶、过滤,则固体乙是硫酸镁晶体
A、9g重水所含有的电子数为5NA
B、1molMgCl5中含有离子数为NA
C、7.1g氯气与足量NaOH溶液反应转移的电子数为0.2NA
D、1molC10H22分子中共价键总数为31NA
A、液体药剂中含不溶性固体药物
B、两种溶液混淆发生化学反响产生积淀
C、改变溶酶性质而
D、使药物拥有局部保护和覆盖创面作用
E、液体药剂中含有毒性药品析出积淀
A、滴定时滴定终点在计量点之前到达
B、滴定时滴定终点在计量点之后到达
C、所称质量中使用的一只10mg砝码,事后发现其校正后的值为9.7mg
D、所称基准物中含有少量的邻苯二甲酸
E、所称基准物未干燥到恒重
“铝热反应”的化学方程式为:2Al+Fe2O3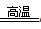 Al2O3+2Fe。某同学对“铝热反应”的现象有这样的描述:“反应放出大量的热,并发出耀眼的光芒”、“纸漏斗的下部被烧穿,有熔融物落入沙中”。查阅《化学手册》知,Al、Al2O3、Fe、Fe2O3熔点、沸点数据如下:
Al2O3+2Fe。某同学对“铝热反应”的现象有这样的描述:“反应放出大量的热,并发出耀眼的光芒”、“纸漏斗的下部被烧穿,有熔融物落入沙中”。查阅《化学手册》知,Al、Al2O3、Fe、Fe2O3熔点、沸点数据如下:
(1)该同学推测,铝热反应所得到的熔融物应是铁铝合金。这种推测有一定的道理,理由是:()。
(2)设计一个简单的实验方案,证明上述所得的块状熔融物中含有金属铝。该实验所用试剂是(),当观察到现象时,说明熔融物中含有金属铝,反应的离子方程式为()。
(3)实验室溶解该熔融物,最好选用下列试剂中的()(填序号)。
A.浓硫酸B.稀硫酸C.稀硝酸D.氢氧化钠溶液