 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)


下列实验现象描述正确的是()
A、锌与稀硫酸反应有大量气泡产生,放出热量
B、氧化铁与稀盐酸反应,溶液由无色变成浅绿色
C、铁在氧气中剧烈燃烧、火星四射,放出大量的热,生成红色固体
D、一氧化碳还原氧化铜,生成黑色固体

 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)


A、锌与稀硫酸反应有大量气泡产生,放出热量
B、氧化铁与稀盐酸反应,溶液由无色变成浅绿色
C、铁在氧气中剧烈燃烧、火星四射,放出大量的热,生成红色固体
D、一氧化碳还原氧化铜,生成黑色固体

 更多“下列实验现象描述正确的是()…”相关的问题
更多“下列实验现象描述正确的是()…”相关的问题
A、打开盛有浓盐酸的试剂瓶,瓶口出现白烟
B、细铁丝在氧气中燃烧,火星四射,生成了四氧化三铁
C、铁锈与稀盐酸反应后溶液颜色由无色变成了黄色
D、将紫色石蕊试液滴入到稀氢氧化钠溶液中变红
A、可选用锌和稀硝酸来制取氢气
B、盛氧化铜的试管应向上倾斜
C、在氢气通入成有氧化铜的试管前要先验纯
D、在氢气还原氧化铜实验结束时,应先撤去通氢气的导管
“铝热反应”的化学方程式为:2Al+Fe2O3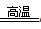 Al2O3+2Fe。某同学对“铝热反应”的现象有这样的描述:“反应放出大量的热,并发出耀眼的光芒”、“纸漏斗的下部被烧穿,有熔融物落入沙中”。查阅《化学手册》知,Al、Al2O3、Fe、Fe2O3熔点、沸点数据如下:
Al2O3+2Fe。某同学对“铝热反应”的现象有这样的描述:“反应放出大量的热,并发出耀眼的光芒”、“纸漏斗的下部被烧穿,有熔融物落入沙中”。查阅《化学手册》知,Al、Al2O3、Fe、Fe2O3熔点、沸点数据如下:
(1)该同学推测,铝热反应所得到的熔融物应是铁铝合金。这种推测有一定的道理,理由是:()。
(2)设计一个简单的实验方案,证明上述所得的块状熔融物中含有金属铝。该实验所用试剂是(),当观察到现象时,说明熔融物中含有金属铝,反应的离子方程式为()。
(3)实验室溶解该熔融物,最好选用下列试剂中的()(填序号)。
A.浓硫酸B.稀硫酸C.稀硝酸D.氢氧化钠溶液
A、细铁丝在氧气中燃烧,火星四射,生成一种黑色固体
B、硫在氧气中燃烧发出明亮的蓝紫色火焰,生成二氧化硫
C、木炭在氧气中燃烧,发出白光,产生大量的热
D、红磷在空气里燃烧,产生大量白烟
A、镁条燃烧:发白光,放热,生成白色固体
B、氧化钙与水反应:白色固体变为白色溶液,放出大量的热
C、电解水:两电极附近产生气泡,一段时间后,正、负极产生气体的体积比约为1:2
D、石蕊溶液滴到氢氧化铝中,溶液不变色
A、浓硫酸和浓盐酸在空气中敞口放置时浓度均减少
B、SO2和Cl2均能使品红溶液褪色
C、浓H2SO4和稀H2SO4与锌反应时均能产生气体
D、HBr、HI气体均不能用浓H2SO4制取
A、②⑤
B、①②③
C、①④⑤
D、④⑤
A、用红磷测定空气中氧气含量的实验中,有大量的白烟产生
B、足量铁粉投入硫酸铜溶液里充分反应后溶液变为无色
C、铁丝在氧气中剧烈燃烧、火星四射、生成白色固体
D、木炭燃烧生成CO2
A、Ⅰ中气体由无色变红棕色的化学方程式为:2NO+O2═2NO2
B、Ⅱ中的现象说明Fe表面形成致密的氧化层,阻止Fe进一步反应
C、对比Ⅰ、Ⅱ中现象,说明稀HNO3的氧化性强于浓HNO3
D、针对Ⅲ中现象,在Fe、Cu之间连接电流计,可判断Fe是否被氧化
A、硫在氧气中燃烧产生微弱的淡蓝色火焰
B、O 通入澄清石灰水,产生白色浑浊
C、棉被在空气中燃烧产生烧焦羽毛气味的气体
D、铁丝在氧气中剧烈燃烧,火星四射,生成黑色固体