 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
下列对实验现象描述错误的是()
A、电解水时正负极产生的气体的体积比为2:1
B、氢氧化钠固体溶于水,溶液温度升高
C、铁丝在氧气中燃烧,生成黑色固体
D、打开盛浓盐酸的试剂瓶,观察到瓶口有白雾出现

 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A、电解水时正负极产生的气体的体积比为2:1
B、氢氧化钠固体溶于水,溶液温度升高
C、铁丝在氧气中燃烧,生成黑色固体
D、打开盛浓盐酸的试剂瓶,观察到瓶口有白雾出现

 更多“下列对实验现象描述错误的是()…”相关的问题
更多“下列对实验现象描述错误的是()…”相关的问题
A、打开盛有浓盐酸的试剂瓶瓶盖,瓶口上方出现白雾
B、向氢氧化钠溶液滴入氯化铁溶液,出现红褐色沉淀
C、镁条在空气中剧烈燃烧,发出耀眼白光
D、硫在空气中燃烧产生明亮的蓝紫色火焰
电解工作原理的实际应用非常广泛。
(1)请画出铜棒镀银的简易装置设计图()。(实验可选用品:铜棒,银片,石墨棒,硫酸铜溶液,硝酸银溶液,导线,电源,烧杯)。
(2)工业上为了处理含有Cr2O12-的酸性工业废水,采用下面的处理方法:往工业废水中加入适量NaCl,以铁为电极进行电解,经过一段时间,有Cr(OH)3和Fe(OH)3沉淀生成,工业废水中铬元素的含量可低于排放标准。关于上述方法,下列说法错误的是()(填字母)。
A、阳极反应:Fe-2e-=Fe2+
B、阴极反应:2H++2e-=H2↑
C、在电解过程中工业废水由酸性变为碱性
D、可以将铁电极改为石墨电极
(3)某同学设计了如图装置进行以下电化学实验。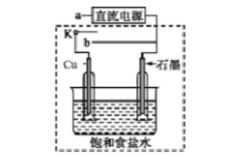 ①当开关K与a连接时,两极均有气泡产生,则阴极为()电极。
①当开关K与a连接时,两极均有气泡产生,则阴极为()电极。
②一段时间后,使开关K与a断开,与b连接时,虚线框内的装置可称为()。请写出此时Cu电极上的电极反应()。
(4)某溶液中含有的离子如下表: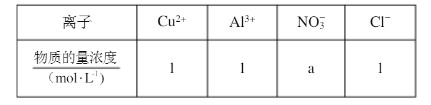 用惰性电极电解该溶液,当电路中有3mole-通过时(忽略电解时溶液体积变化及电极产物可能存在的溶解现象),下列说法正确的是()(填字母)。
用惰性电极电解该溶液,当电路中有3mole-通过时(忽略电解时溶液体积变化及电极产物可能存在的溶解现象),下列说法正确的是()(填字母)。
A、电解后溶液呈酸性
B、a=3
C、阳极生成1.5molCl2
D、阴极析出的金属是铜与铝
A、红磷在空气中燃烧,产生大量白雾
B、硫在氧气中燃烧会产生明亮的蓝紫色火焰,生成有刺激性气味的气体
C、木炭在空气中燃烧发出白光,放热,生成一种能使澄清石灰水变浑浊的气体
D、铁丝在氧气中燃烧,火星四射,生成黑色的四氧化三铁
A、②⑤
B、①②③
C、①④⑤
D、④⑤
下列有关DRIs描述错误的是()。
A、平均需要量可以满足群体中50个体的需要
B、RNI是可以满足某一群体中100个体的需要量
C、AI和RNI都可以作为个体摄入量的目标
D、AI是通过对健康人群摄入量的观察或实验获得的
A、用红磷测定空气中氧气含量的实验中,有大量的白烟产生
B、足量铁粉投入硫酸铜溶液里充分反应后溶液变为无色
C、铁丝在氧气中剧烈燃烧、火星四射、生成白色固体
D、木炭燃烧生成CO2
“铝热反应”的化学方程式为:2Al+Fe2O3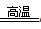 Al2O3+2Fe。某同学对“铝热反应”的现象有这样的描述:“反应放出大量的热,并发出耀眼的光芒”、“纸漏斗的下部被烧穿,有熔融物落入沙中”。查阅《化学手册》知,Al、Al2O3、Fe、Fe2O3熔点、沸点数据如下:
Al2O3+2Fe。某同学对“铝热反应”的现象有这样的描述:“反应放出大量的热,并发出耀眼的光芒”、“纸漏斗的下部被烧穿,有熔融物落入沙中”。查阅《化学手册》知,Al、Al2O3、Fe、Fe2O3熔点、沸点数据如下:
(1)该同学推测,铝热反应所得到的熔融物应是铁铝合金。这种推测有一定的道理,理由是:()。
(2)设计一个简单的实验方案,证明上述所得的块状熔融物中含有金属铝。该实验所用试剂是(),当观察到现象时,说明熔融物中含有金属铝,反应的离子方程式为()。
(3)实验室溶解该熔融物,最好选用下列试剂中的()(填序号)。
A.浓硫酸B.稀硫酸C.稀硝酸D.氢氧化钠溶液
A、细铁丝在氧气中燃烧,火星四射,生成一种黑色固体
B、硫在氧气中燃烧发出明亮的蓝紫色火焰,生成二氧化硫
C、木炭在氧气中燃烧,发出白光,产生大量的热
D、红磷在空气里燃烧,产生大量白烟
A、打开盛有浓盐酸的试剂瓶,瓶口出现白烟
B、细铁丝在氧气中燃烧,火星四射,生成了四氧化三铁
C、铁锈与稀盐酸反应后溶液颜色由无色变成了黄色
D、将紫色石蕊试液滴入到稀氢氧化钠溶液中变红