 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)


下列变化中属于吸热反应的是()①铝片与稀盐酸的反应 ②Ba(OH)2·8H2O与NH4Cl的反应 ③干冰汽化 ④氯酸钾分解制氧气 ⑤Al与Fe2O3高温下反应(铝热反应)
A、①④
B、②③
C、①④⑤
D、②④

 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)


A、①④
B、②③
C、①④⑤
D、②④

 更多“下列变化中属于吸热反应的是()①铝片与稀盐酸的反…”相关的问题
更多“下列变化中属于吸热反应的是()①铝片与稀盐酸的反…”相关的问题
A、l与Fe2O3的铝热反应属于放热反应
B、NaOH+HCl=NaCl+H2O不能实现化学能转化为电能的理由是反应太快,形成电流时间短暂
C、Ba(OH)2·8H2O与NH4Cl的反应属于吸热反应
D、反应物的总能量低于生成物的总能量,反应时从环境吸收能量
A、稀硝酸与氢氧化钾溶液反应H++OH-→H2O
B、铝与稀盐酸反应Al+2H+→Al3++H2↑
C、氯化铁溶液与氢氧化钠溶液反应FeCl3+3OH-→Fe(OH)3↓+3C1-
D、二氧化碳与石灰水反应CO2+2OH-→CO32-+H2O
A、浓硫酸和浓盐酸在空气中敞口放置时浓度均减少
B、SO2和Cl2均能使品红溶液褪色
C、浓H2SO4和稀H2SO4与锌反应时均能产生气体
D、HBr、HI气体均不能用浓H2SO4制取
“铝热反应”的化学方程式为:2Al+Fe2O3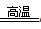 Al2O3+2Fe。某同学对“铝热反应”的现象有这样的描述:“反应放出大量的热,并发出耀眼的光芒”、“纸漏斗的下部被烧穿,有熔融物落入沙中”。查阅《化学手册》知,Al、Al2O3、Fe、Fe2O3熔点、沸点数据如下:
Al2O3+2Fe。某同学对“铝热反应”的现象有这样的描述:“反应放出大量的热,并发出耀眼的光芒”、“纸漏斗的下部被烧穿,有熔融物落入沙中”。查阅《化学手册》知,Al、Al2O3、Fe、Fe2O3熔点、沸点数据如下:
(1)该同学推测,铝热反应所得到的熔融物应是铁铝合金。这种推测有一定的道理,理由是:()。
(2)设计一个简单的实验方案,证明上述所得的块状熔融物中含有金属铝。该实验所用试剂是(),当观察到现象时,说明熔融物中含有金属铝,反应的离子方程式为()。
(3)实验室溶解该熔融物,最好选用下列试剂中的()(填序号)。
A.浓硫酸B.稀硫酸C.稀硝酸D.氢氧化钠溶液
A、向滴有酚酞的Na2CO3溶液中加入BaCl2溶液,溶液褪色,说明BaCl2有酸性
B、H2S能与CuSO4溶液反应生成H2SO4,说明氢硫酸的酸性比硫酸强
C、用玻璃棒蘸取浓氨水点到红色石蕊试纸上,试纸变蓝色,说明浓氨水呈碱性
D、常温下,将铝片放入浓硫酸中,无明显现象,说明铝不与冷的浓硫酸发应