 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
某有机物m g,与足量金属钠反应生成V L H2,另取m g该有机物与足量碳酸氢钠作用生成V L CO2(相同状况下),该有机物分子中含有的官能团可能为()
A、一个羧基和一个羟基
B、两个羟基
C、一个羧基
D、两个羧基

 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A、一个羧基和一个羟基
B、两个羟基
C、一个羧基
D、两个羧基

 更多“某有机物m g,与足量金属钠反应生成V L H2…”相关的问题
更多“某有机物m g,与足量金属钠反应生成V L H2…”相关的问题
A、某有机物完全燃烧,只生成CO2和H2O, 结论:该有机物属于烃类物质
B、乙醇和水都可与金属钠反应产生可燃性气体, 结论:乙醇分子中的氢与水分子中的氢具有相同的活性
C、用乙酸浸泡水壶中的水垢,可将其清除, 结论:乙酸的酸性强于碳酸的酸性
D、甲烷与氯气在光照下反应后的混合气体能使湿润的石蕊试纸变红, 结论:生产的氯代甲烷具有酸性
A、某有机物燃烧只生成CO₂和H₂O,且二者物质的量相等,则此有机物的组成为CnH2n
B、一种烃在足量的氧气中燃烧并通过浓硫酸,减少的总体积就是生成的水蒸气的体积
C、某气态烃CxHy与足量O₂恰好完全反应(温度>100℃),如果反应前后气体体积不变,则y=4;若体积减小,则y>4;若体积增大,则y<4
D、相同质量的烃,完全燃烧,消耗O₂越多,烃中含H量越高
A、1molC2H4Cl2中含有共用电子对数目为7NA
B、标准状况下,44.8L丙三醇与足量金属钠反应,生成气体的分子数为3NA
C、20℃时,1mol己烷完全燃烧后恢复至原状态,生成气态物质分子数为6NA
D、15g甲基正离子(CH3+)所含有的电子数是8NA
A、2.3 g钠与97.7 g水反应后,溶液中溶质的质量分数等于4%
B、钠和CuSO4溶液反应生成的蓝色沉淀上有时出现暗斑,这是析出了金属铜
C、向金属钠与水反应后的溶液中通入适量氯气后,溶液中含有两种溶质
D、钠在空气中的缓慢氧化与其在空气中点燃所得的产物一样
A、8.64
B、9.20
C、9.00
D、9
A、6∶3∶2
B、1∶2∶3
C、3∶2∶1
D、4∶3∶2
A、乙酸与乙醇可以发生酯化反应,又均可与金属钠发生置换反应
B、乙烯、氯乙烯、聚乙烯均可使酸性高锰酸钾溶液褪色
C、分馏、干馏都是物理变化,裂化、裂解都是化学变化
D、纤维素、聚乙烯、光导纤维都属于高分子化合物
A、9.0L
B、13.5L
C、15.7L
D、16.8L
我国是世界产镁大国,金属镁的产量居世界前列。一种由白云石(主要成分为CaO▪MgO,含少量SiO2、A12O3、Fe2O3等杂质)冶炼金属镁的工艺流程如图: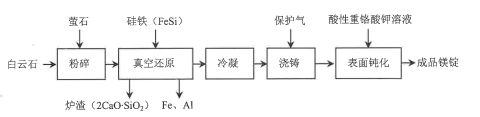 已知:萤石的主要成分是CaF2,用于降低真空还原反应的活化能。
已知:萤石的主要成分是CaF2,用于降低真空还原反应的活化能。
回答下列问题:
(1)①粉碎的主要目的()。
②萤石在真空还原反应中的作用是()(填标号)。
A.氧化剂B.还原剂C.催化剂
(2)Mg2+、Ca2+、Fe3+、Fe2+、A13+五种离子的氧化性由强到弱的顺序为Fe3+>Fe2+>()(用离子符号表示)。
(3)结合流程以及如图温度对MgO还原率的影响关系,真空还原反应温度的最佳选择为();高温真空还原时,CaO、MgO和FeSi反应生成单质镁的化学方程式为()。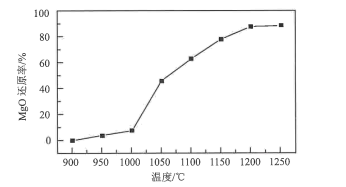 (4)液态镁浇铸成镁锭时,通入的保护气不可选用N2或CO2,其原因是()。
(4)液态镁浇铸成镁锭时,通入的保护气不可选用N2或CO2,其原因是()。
(5)镁锭冷却后,用酸性K2Cr2O7溶液进行表面钝化形成致密的氧化物保护膜,还原产物为Cr3+。该反应的离子方程式为()。
(6)为测定镁锭的纯度,称取a()g除去氧化膜的成品镁锭样品溶于足量稀硫酸中,配成250mL溶液。取25mL该溶液,用0.1000mol/L的EDTA标准溶液进行滴定(杂质不干扰滴定),三次滴定平均消耗EDTA标准溶液V()mL(己知Mg2+与EDTA反应的化学计量数之比为1:1)。该样品的纯度为()%。