 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
水分子中两个H-O键之间的键角为()。
A、104°40’
B、107°32’
C、112°12’
D、114°04’

 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A、104°40’
B、107°32’
C、112°12’
D、114°04’

 更多“水分子中两个H-O键之间的键角为()。…”相关的问题
更多“水分子中两个H-O键之间的键角为()。…”相关的问题
A、H2S分子中两个共价键的键角接近90度的原因是共价键有方向性
B、N2分子中有1个σ键两个π键
C、在双键中,σ键的键能小于π键的键能
D、两个原子形成共价键时至少有1个σ键
A、CH3Cl只有一种结构
B、CH2Cl2只有一种结构
C、CHCl3只有一种结构
D、CH4中四个价键的键角和键长都相等
A、PCl3分子中三个共价键的键长和键角都相等
B、PCl3分子中的P-Cl键属于极性共价键
C、PCl3分子中三个共价键键能相等
D、PCl3分子中磷原子是sp2杂化
A、键能均相等
B、键角均为109°28′
C、有两种同分异构体
D、该分子共含电子总数为42
正四面体烷是一种可能存在的柏较图轻,IUPAC名称为三环U.I.0.0丁烷。其球棍模型如图所示。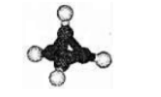 下列关于该化合物的说法正确的是()。
下列关于该化合物的说法正确的是()。
A、与环丁二烯互为同分异构体
B、二氯代物超过两种
C、碳碳键键角为109。28'
D、三环[1.1.0.0]丁烷生成1mol丁烷至少需要2molH2
A、原子轨道的杂化,只有在形成分子的过程中才会发生,而孤立的原子是不可能发生杂化的
B、只有能量相近的原子轨道才能发生杂化
C、一定数目的原子轨道杂化后,可以得到更多数量的杂化轨道
D、CH4分子中有四个能量相等的C—H键,键角为109°28′,分子的空间构型为正四面体,这一情况可以用杂化轨道理论解释
A、含有三个碳碳双键和三个碳碳单键
B、分子中6个碳碳键完全相同
C、所有碳原子都在同一平面上,氢原子不在该平面上
D、每两个键之间的夹角都为60°