 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
下列溶液中能大量共存的离子组是()。
A、H+、Fe2+、Cl-、NO3-
B、NH4+、SO42-、Na+、OH-
C、Cu2+、Fe3+、NO3-、Cl-
D、H+、Na+、HCO3-、SO42-

 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A、H+、Fe2+、Cl-、NO3-
B、NH4+、SO42-、Na+、OH-
C、Cu2+、Fe3+、NO3-、Cl-
D、H+、Na+、HCO3-、SO42-

 更多“下列溶液中能大量共存的离子组是()。…”相关的问题
更多“下列溶液中能大量共存的离子组是()。…”相关的问题
A、S2-、Na+、ClO-、OH-
B、Na+、HCO3-、Cl-、H+
C、Na+、Al3+、Cl-、SO42-
D、H+、Fe2+、NO3-、SO42-
A、K+,HCO3-,Cl-,SO42-
B、S2-,CO32-,Cl-,K+
C、K+,Cu2+,SO42-,Na+
D、K+,Cs+,NO3-,SO42-
A、AgNO,NaCl,KNO3
B、Ba(NO3)2,HCl,Na2SO4
C、NH4Cl,NaOH,NaNO3
D、KNO3,NaNO3,HCl
A、甲、乙两溶液的pH不可能相同
B、甲、乙两种溶液中加入Al粉都一定会产生H2
C、HCO3-不可能在甲、乙两溶液中大量共存
D、甲不可能是盐溶液,乙不可能是酸或碱溶液
A、0.2mol/L的NH4Cl溶液:Na+、K+、SO4²-、AlO₂-
B、0.1mol/L的FeCl₃溶液:NH4+、Ca²+、Br-、SCN-
C、0.2mol/L的H₂SO4溶液:Mg2+、Fe²+、NO₃-、Cl-
D、0.1mol/L的Ba(OH)₂溶液:Na+、K+、Cl-、ClO-
生产上用过量烧碱溶液处理某矿物(含Al2O3、MgO),过滤后得到的滤液用NaHCO3溶液处理,测得溶液pH、n[Al(OH)3]随加入NaHCO3溶液体积变化的曲线如下图所示。下列有关说法不正确的是()。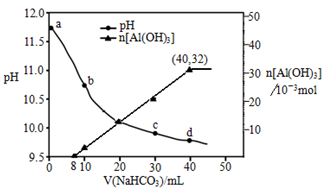
A、生成沉淀的离子方程式为HCO3-+AlO2-+H2O=Al(OH)3↓+CO32-
B、b点与c点溶液所含微粒种类相同
C、a点溶液中大量存在的离子是Na+、AlO2-、OH-
D、NaHCO3溶液的物质的量浓度为0.8mol/L
A、通过沉淀反应,可以使溶液中某种离子的浓度变为0
B、反应NH3+H3O+NH4++H2O能自发进行,说明NH3结合H+能力比H2O强
C、若测得雨水的pH小于7,则下的是酸雨
D、先将pH试纸用蒸馏水润湿后,再测定溶液的pH