 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)


戴维孙一革末实验中以电子射向晶体镍的表面,该实验用来A.测定电子的荷质比B.确认光电效应的真实
戴维孙一革末实验中以电子射向晶体镍的表面,该实验用来
A.测定电子的荷质比
B.确认光电效应的真实性
C.表明电子的波动性
D.观察到原子能级的不连续性
E.证明电子具有自旋
请帮忙给出正确答案和分析,谢谢!

 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)


戴维孙一革末实验中以电子射向晶体镍的表面,该实验用来
A.测定电子的荷质比
B.确认光电效应的真实性
C.表明电子的波动性
D.观察到原子能级的不连续性
E.证明电子具有自旋
请帮忙给出正确答案和分析,谢谢!

 更多“戴维孙一革末实验中以电子射向晶体镍的表面,该实验…”相关的问题
更多“戴维孙一革末实验中以电子射向晶体镍的表面,该实验…”相关的问题
A、高锰酸钾是一种常用的化学试剂,当高锰酸钾晶体结块时,应在研钵中用力研磨,以得到细小晶体,有利于加快反应或溶解的速率
B、检验某溶液是否含有SO时,应取少量该溶液,依次加入稀盐酸和BaCl2溶液
C、为观察镁条在CO2气体中的燃烧,在一个底部铺有少量玻璃棉的集气瓶中收集满CO2气体,取一小段除去表面氧化膜的镁条用坩埚钳夹持点燃后迅速投入上述集气瓶底部
D、用干燥且洁净的玻璃棒蘸取NaClO溶液,点到放在表面皿上的pH试纸上测其pH
从含镍废催化剂中可回收镍,其流程如下: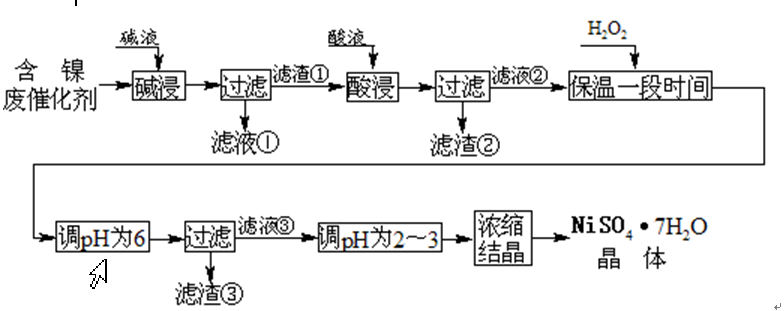 某油脂化工厂的含镍催化剂主要含有Ni,还含有Al(31%)、Fe(1.3%)的单质及氧化物,其他不溶杂质(3.3%)。部分阳离子以氢氧化物形式完全沉淀时的pH如下
某油脂化工厂的含镍催化剂主要含有Ni,还含有Al(31%)、Fe(1.3%)的单质及氧化物,其他不溶杂质(3.3%)。部分阳离子以氢氧化物形式完全沉淀时的pH如下
问题一、碱浸“的目的是除去()。
问题二、“酸浸”时所加入的酸是()(填化学式)。酸浸后,滤液②中可能含有的金属离子是()。
问题三、“调pH为2~3”的目的是()。
问题四、产品晶体中有时会混有少量绿矾(FeSO4•7H2O),可能是由于生产过程中()导致Fe2+未被完全氧化造成的。
问题五、NiSO4在强碱溶液中用NaClO氧化,可制得碱性镍镉电池电极材料——NiOOH。该反应的离子方程式是()
氯化镁是重要的无机材料,在常温下易吸湿,可溶于水和乙醇。某兴趣小组以海水为原料制备无水氯化镁。
实验一制备MgCl2·6H2O晶体
以海水为原料,对其进行一系列处理,得到晶体。
(1)除去海水中不溶性杂质常用的实验操作是()(填名称)。
(2)从氯化镁溶液中析出MgCl2·6H2O晶体的结晶方法是()(填“降温结晶”或“蒸发结晶”)。
实验二样品中MgCl2·6H2O晶体含量测定
准确称取实验一制得的MgCl2·6H2O晶体ag于锥形瓶中,加去离子水溶解,依次加入一定量三乙醇胺、NH3-NH4Cl缓冲溶液,摇匀,滴入铬黑T指示剂,用0.02000mol·L-1EDTA(用H2Y2-表示)标准溶液滴定至终点,消耗EDTA溶液的体积VmL。
已知:①0.02000mol·L-1EDTA标准溶液pH约为5,指示剂铬黑T使用的适宜pH范围为8~11,NH3-NH4Cl缓冲溶液pH约为10。
②滴定原理: Mg2++H2Y2-=MgY2-+2H+。
(3)使用的滴定管是()(填“甲”或“乙”)。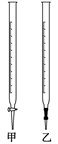 (4)NH3-NH4Cl缓冲溶液的作用是()。
(4)NH3-NH4Cl缓冲溶液的作用是()。
(5)样品中MgCl2·6H2O的质量分数为()。
实验三制备无水氯化镁
利用如图实验装置(夹持和加热装置省略),准确称取一定质量MgCl2·6H2O晶体在HCl气流中小心加热。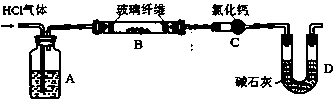 (6)A装置的作用是()。
(6)A装置的作用是()。
(7)某同学在实验前后测得玻璃管B减重m1g,干燥管C增重m2g,m1>m2,其可能的原因是()(用化学方程式表示)。
A、汤姆孙通过研究阴极射线实验,发现了电子
B、卢瑟福通过对α粒子散射实验现象的分析,证实了原子是可以再分的
C、查德威克通过对α粒子散射实验现象的分析,提出了原子的核式结构模型
D、玻尔根据氢原子光谱分析,总结出了氢原子光谱可见光区波长公式
A、皮制家具
B、木质家具
C、布制家具
D、革制家具
A、卢瑟福提出枣糕原子模型
B、汤姆孙发现电子,表明原子具有核式结构
C、汤姆孙通过研究阴极射线实验,发现了电子的存在
D、卢瑟福通过对α粒子散射实验现象的分析,证实了原子是可以再分的
A、在晶体膜表面氧化而传递电子;
B、在晶体膜表面进行离子交换和扩散形成双电层结构;
C、穿透晶体膜使膜内外氟离子产生浓度差形成双电层结构;
D、进入晶体膜表面的晶格缺陷形成双电层结构。